
在健康消费升级的浪潮中,药食同源食材凭借“天然安全、温和调理” 的独特优势,成为食品行业创新研发的核心方向。湖北嫦娥生物股份有限公司深耕健康领域,精准把握市场需求,将薏苡仁这一传承千年的药食同源佳品纳入核心配料,以传统智慧结合现代工艺,为消费者带来兼顾美味与健康的全新选择。
图源:国家卫生健康委员会政务服务平台网站
发表于国际权威期刊Frontiers in Nutrition上的一篇重磅研究Effects of Coix Seed Extract, Bifidobacterium BPL1, and Their Combination on the Glycolipid Metabolism in Obese Mice(doi: 10.3389/fnut.2022.939423),通过严谨的动物实验,从科学层面深度解码了薏苡仁调节糖脂代谢的神奇功效,让这一古老食材在现代健康领域焕发璀璨新生。

薏苡仁(Coix Seed),俗称薏米、薏仁,作为禾本科薏苡属植物的干燥成熟种仁,在我国的食用与药用历史可追溯至数千年前。中医经典《神农本草经》将其列为上品,记载其“利水渗湿、健脾止泻、活血祛瘀” 的功效;《本草纲目》亦赞其 “健脾益胃,补肺清热,去风渗湿”。在中医体质理论中,薏苡仁尤其适合痰湿质、气虚质、痰湿兼血瘀质等与肥胖相关的偏颇体质调理,这与现代研究中薏苡仁调节代谢的功效不谋而合。从营养成分来看,薏苡仁富含多糖(含量≥30%)、不饱和脂肪酸、酯类、蛋白质、多酚等多种活性物质,这些成分正是其发挥生理功效的核心基础。

现代社会,高脂高糖的饮食结构、缺乏运动的生活方式,让糖脂代谢紊乱成为困扰全球人群的健康难题。2022年,世界卫生组织的数据显示,有25亿成人超重,其中超过8.9亿成人患有肥胖症。糖脂代谢紊乱不仅会导致体重超标,还可能引发胰岛素抵抗、脂肪肝、高血脂、高血压等一系列代谢性疾病,严重威胁人体健康。常规的药物调理往往存在副作用,且依从性较差,而薏苡仁作为天然药食同源食材,其温和的调理特性和显著的代谢调节效果,为解决这一健康痛点提供了新的思路。
研究人员通过严格的动物实验验证了薏苡仁调节糖脂代谢的显著功效。研究团队选取150只C57BL/6J雄性小鼠,经8周高脂饲料喂养构建肥胖模型后,将成功建模的小鼠分为模型对照组和三个干预组,进行为期10周的连续灌胃干预。实验结果(如下图1-2)显示,薏苡仁提取物干预组的小鼠体重较模型组(42.23g)降低约2.31g,附睾脂肪含量较模型组(2.5g)减少0.37g,肾周脂肪含量较模型组(0.884g)减少0.47g,脂肪蓄积得到有效抑制。更值得关注的是,薏苡仁提取物对脂肪分布的调节具有针对性,其减少皮下脂肪的效果尤为突出,能有效改善肥胖小鼠的体型特征。
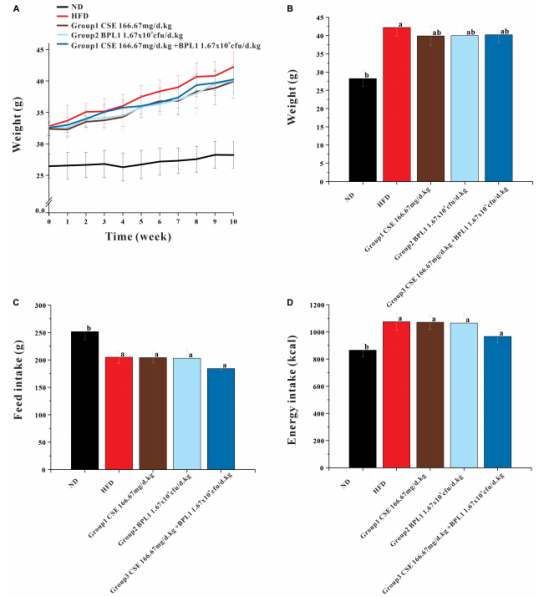
图1 小鼠体重及采食量检测结果
(A) 干预期间小鼠体重变化;(B) 各组小鼠干预结束时体重;(C) 小鼠总采食量;(D) 小鼠总能量摄入量。数据以均值 ± 标准差表示(n=12)。a:与正常对照组(ND)相比,P<0.05;b:与高脂模型组(HFD)相比,P<0.05。
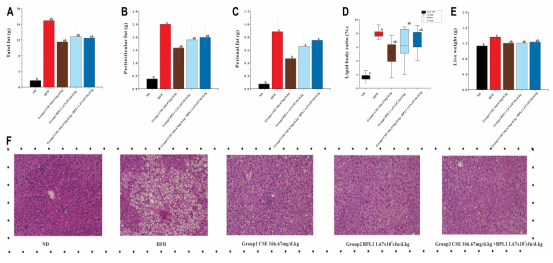
图2 小鼠体脂分布检测结果
(A) 小鼠体脂总重量;(B) 附睾脂肪重量;(C) 肾周脂肪重量;(D) 脂体比;(E) 肝脏重量;(F) 肝脏组织苏木精-伊红(HE)染色结果。数据以均值 ± 标准差表示(n=12)。a:与正常对照组(ND)相比,P<0.05;b:与高脂模型组(HFD)相比,P<0.05。
在血糖调节方面,研究数据(如下图3)呈现出清晰的改善趋势:高脂模型组小鼠空腹血糖呈缓慢上升态势,而薏苡仁提取物干预组从第4周开始,空腹血糖便显著低于模型组(P<0.05),且持续下降。口服葡萄糖耐量试验显示,薏苡仁提取物干预组的血糖曲线下面积(AUC)显著小于模型组,表明其能有效提升机体对葡萄糖的耐受能力和调节能力。同时,干预组小鼠的血清胰岛素水平升高,胰岛素抵抗指数(HOMA-IR)降低,胰岛β细胞功能指数(HOMA-β)升高,且与正常对照组接近,说明薏苡仁提取物能有效保护胰岛功能,缓解胰岛素抵抗,从根源上改善血糖代谢异常。实验结束时,薏苡仁提取物单一组对空腹血糖的控制效果在各干预组中表现最佳,充分证明了其在降糖方面的独特优势。
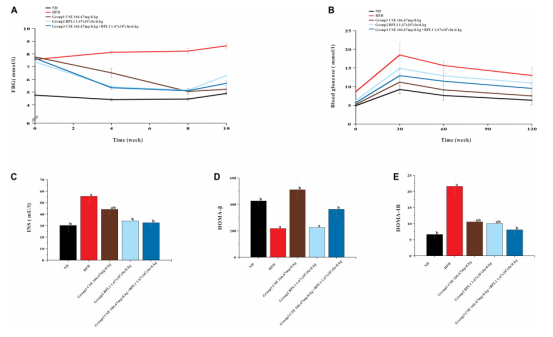
图3 小鼠糖代谢相关指标检测结果
(A) 空腹血糖;(B) 口服葡萄糖耐量试验(OGTT);(C) 血清胰岛素(INS)水平;(D) 胰岛β细胞功能指数(HOMA-β);(E) 胰岛素抵抗指数(HOMA-IR)。
血脂调节方面,如下图4,高脂饮食导致模型组小鼠血清总胆固醇(TC)、甘油三酯(TG)、极低密度脂蛋白(VLDL)水平显著升高,高密度脂蛋白(HDL)水平降低,呈现典型的血脂紊乱特征。而经薏苡仁提取物干预后,肥胖小鼠的血清TG、TC、VLDL水平显著下降,HDL水平明显升高,血脂谱得到全面改善。其中,薏苡仁提取物提升HDL的效果优于双歧杆菌BPL1单一组,而HDL作为 “好胆固醇”,对保护血管健康、预防动脉粥样硬化具有重要意义,这一发现进一步凸显了薏苡仁在心血管健康保护方面的价值。
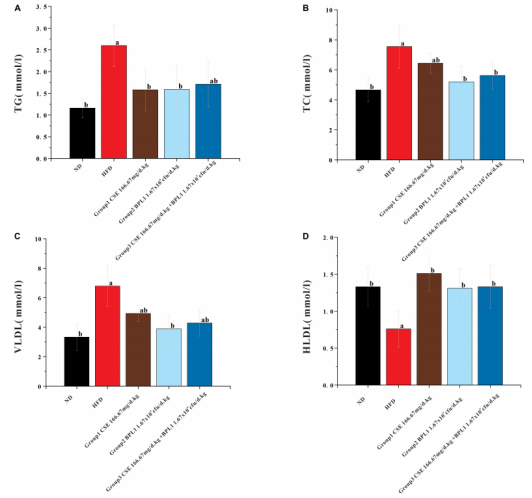
图4 小鼠血脂水平检测结果
(A) 甘油三酯(TG);(B) 总胆固醇(TC);(C) 极低密度脂蛋白(VLDL);(D) 高密度脂蛋白(HDL)。数据以均值 ± 标准差表示(n=12);a:与正常对照组(ND)相比,P<0.05;b:与高脂模型组(HFD)相比,P<0.05。
薏苡仁调节糖脂代谢的机制复杂而精妙,如下图5,研究揭示其主要通过多重路径协同作用。首先是抗炎路径,慢性低度炎症是导致胰岛素抵抗和糖脂代谢紊乱的关键因素,肥胖会引发内质网应激,激活NF-κB、JNK等炎症通路,导致IL-1β、TNF-α等炎症因子释放增加。薏苡仁提取物能直接作用于机体组织,降低血清中IL-1β和TNF-α的水平,缓解慢性炎症状态,从而改善胰岛素敏感性,提升机体对葡萄糖的利用能力。
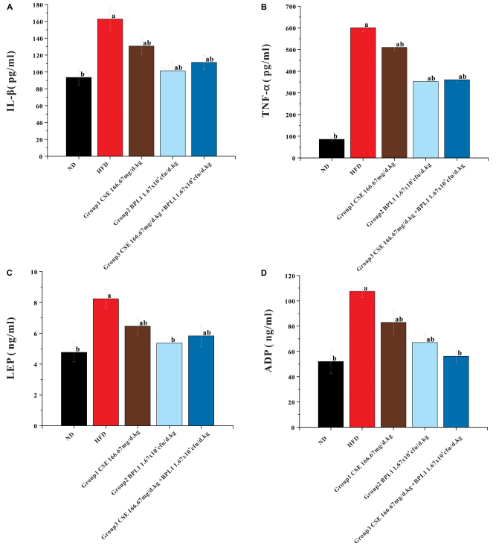
图5 小鼠血清糖脂代谢相关指标检测结果
(A) 炎症因子白细胞介素-1β(IL-1β);(B) 炎症因子肿瘤坏死因子-α(TNF-α);(C) 血清瘦素(LEP)水平;(D) 血清脂联素(ADP)水平。数据以均值 ± 标准差表示(n=12);a:与正常对照组(ND)相比,P<0.05;b:与高脂模型组(HFD)相比,P<0.05。
其次是脂质合成抑制路径,如下图6,薏苡仁中的活性成分能调控脂质代谢相关蛋白的表达,显著降低肝脏组织中脂肪酸合成酶(FAS)、固醇调节元件结合转录因子(SREBP-1c)、脂蛋白脂酶(LPL)等的蛋白水平,抑制脂肪合成与蓄积。同时,薏苡仁还能通过调节脂联素-腺苷酸活化蛋白激酶-乙酰辅酶A羧化酶-丙二酰辅酶A-游离脂肪酸代谢通路,减少血液中游离脂肪酸含量,增加抗氧化酶活性,降低血清自由基水平,进一步辅助调节脂质代谢。
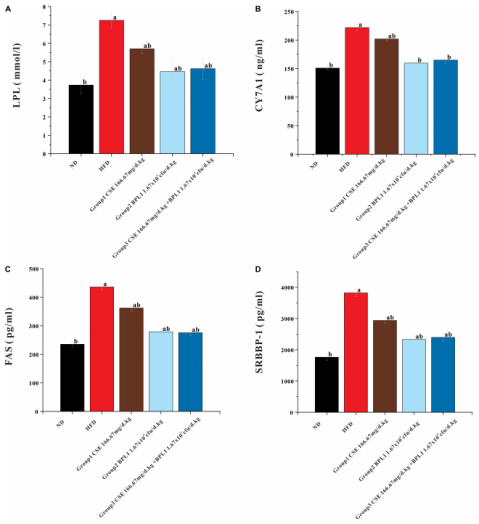
图6 小鼠肝脏组织糖脂代谢相关指标检测结果
(A) 脂蛋白脂酶(LPL);(B) 脂肪酸合成酶(FAS);(C) 胆固醇7α-羟化酶(CYP7A1);(D) 固醇调节元件结合转录因子 1(SREBP-1)。数据以均值 ± 标准差表示(n=12)。a:与正常对照组(ND)相比,P<0.05;b:与高脂模型组(HFD)相比,P<0.05。
肠道菌群调节是薏苡仁发挥代谢调理作用的另一重要路径。肠道菌群平衡与代谢健康密切相关,肥胖小鼠的肠道菌群结构存在明显异常,厚壁菌门、变形菌门占比升高,拟杆菌门占比降低,乳球菌属等有害菌丰度增加。如下图7,研究发现,薏苡仁提取物虽未直接改变抗炎相关菌群的丰度,但与益生菌联合使用时,能协同调节肠道菌群结构,显著增加双歧杆菌等有益菌丰度,减少与肥胖相关的乳球菌属,改善肠道菌群多样性和功能,进而增强糖脂代谢调节效果。此外,薏苡仁还能保护肠道黏膜免疫功能,修复肠道屏障,促进降糖信号通路传导,为代谢健康提供肠道层面的保障。
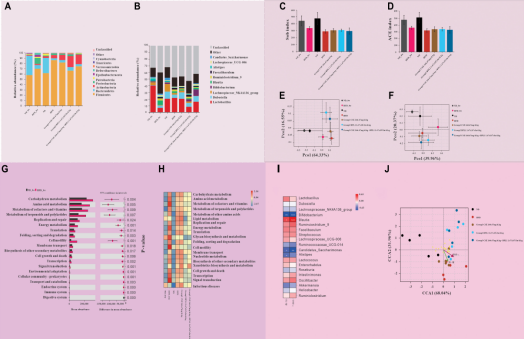
图7 小鼠肠道菌群检测结果
(A、B) 肠道菌群组成分布:(A) 门水平;(B) 属水平(C~F) 肠道菌群多样性分析:(C) 肠道菌群α多样性Sob指数;(D) 肠道菌群α多样性 ACE 指数;(E) 门水平肠道菌群β多样性;(F) 属水平肠道菌群β多样性(G、H) 肠道菌群功能分析:(G) 干预初期肥胖小鼠与正常小鼠的菌群功能对比;(H) 干预结束后各组小鼠的菌群功能对比(I、J) 炎症因子与肠道菌群的关联性分析:(I) 肠道菌群与炎症因子的相关性;(J) 不同组别肠道菌群与炎症因子的关联关系
能量代谢提升也是薏苡仁的重要作用机制之一。研究显示,肥胖模型小鼠的能量消耗底物主要为脂肪,对葡萄糖的利用能力低下,表现为呼吸交换率(RER)稳定在0.76左右(接近脂肪代谢的特征值)。而薏苡仁提取物干预后,小鼠的呼吸交换率升高,表明葡萄糖在能量代谢底物中的占比增加,机体能量利用效率提升。同时,薏苡仁提取物能增加肥胖小鼠的自主活动量,提升活动能量消耗,进一步促进脂肪分解,减少脂肪堆积。
在中医理论中,薏苡仁的“健脾祛湿” 功效与现代研究的 “调节代谢” 作用高度契合,体现了传统智慧与现代科学的殊途同归。随着人们健康意识的不断提升,天然、安全、有效的调理方式成为主流需求。薏苡仁作为兼具美味与功效的药食同源食材,在科学研究的加持下,其调节糖脂代谢的功效得到充分证实。选择含薏苡仁的健康食品,就是选择一种温和、持久、天然的健康生活方式,让身体在日常饮食中回归平衡,焕发活力。
特别声明:本文仅为原料相关的科普分享,不涉及任何产品的功效宣传,亦不构成对疾病治疗的相关宣称。


